Benchmarks
View scores and output across OCR models spanning many document categories.
Want to run these evals on your own documents?
Talk to Sales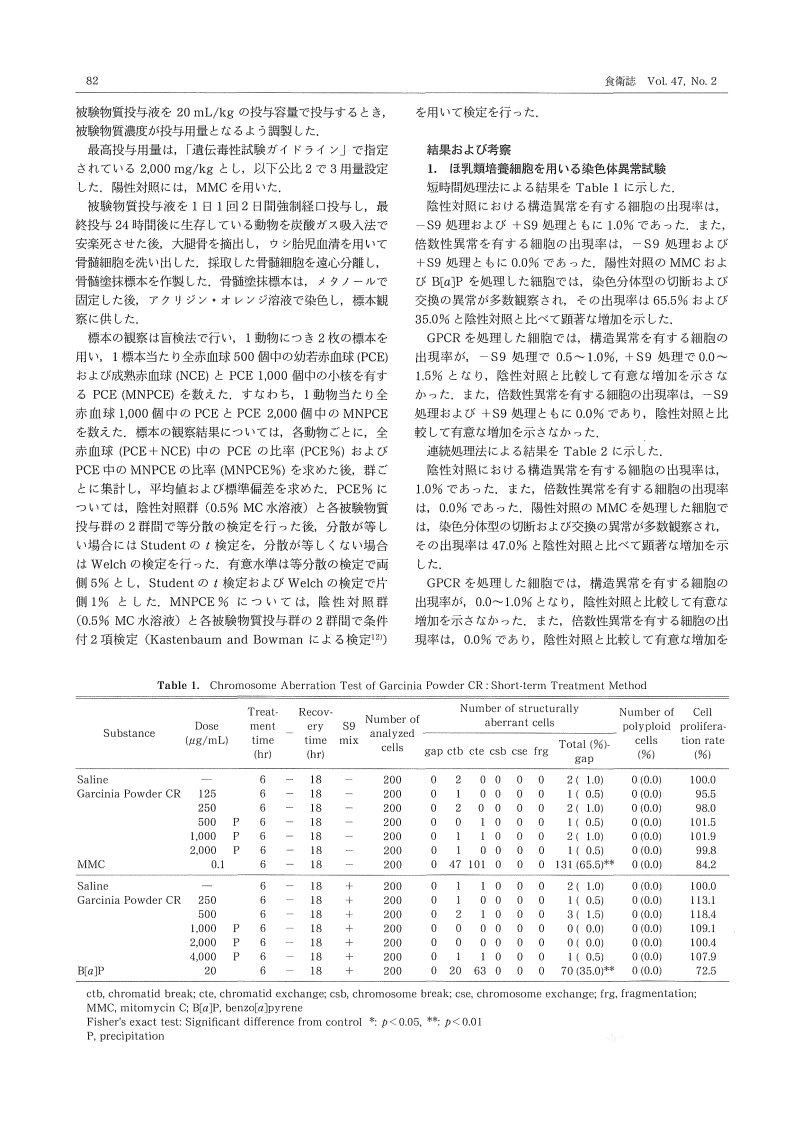
82
食衛誌 Vol. 47, No. 2
被験物質投与液を 20 mL/kg の投与容量で投与するとき、被験物質濃度が投与用量となるよう調製した。
最高投与用量は、「遺伝毒性試験ガイドライン」で指定されている 2,000 mg/kg とし、以下公比 2 で 3 用量設定した。陽性対照には、MMC を用いた。
被験物質投与液を 1 日 1 回 2 日間強制経口投与し、最終投与 24 時間後に生存している動物を炭酸ガス吸入法で安楽死させた後、大腿骨を摘出し、ウシ胎児血清を用いて骨髄細胞を洗い出した。採取した骨髄細胞を遠心分離し、骨髄塗抹標本を作製した。骨髄塗抹標本は、メタノールで固定した後、アクリジン・オレンジ溶液で染色し、標本観察に供した。
標本の観察は盲検法で行い、1 動物につき 2 枚の標本を用い、1 標本当たり全赤血球 500 個中の幼若赤血球 (PCE) および成熟赤血球 (NCE) と PCE 1,000 個中の小核を有する PCE (MNPCE) を数えた。すなわち、1 動物当たり全赤血球 1,000 個中の PCE と PCE 2,000 個中の MNPCE を数えた。標本の観察結果については、各動物ごとに、全赤血球 (PCE+NCE) 中の PCE の比率 (PCE%) および PCE 中の MNPCE の比率 (MNPCE%) を求めた後、群ごとに集計し、平均値および標準偏差を求めた。PCE% については、陰性対照群 (0.5% MC 水溶液) と各被験物質投与群の 2 群間で等分散の検定を行った後、分散が等しい場合には Student の t 検定を、分散が等しくない場合は Welch の検定を行った。有意水準は等分散の検定で両側 5% とし、Student の t 検定および Welch の検定で片側 1% とした。MNPCE% については、陰性対照群 (0.5% MC 水溶液) と各被験物質投与群の 2 群間で条件付 2 項検定 (Kastenbaum and Bowman による検定 12) )
を用いて検定を行った。
結果および考察
1. ほ乳類培養細胞を用いる染色体異常試験
短時間処理法による結果を Table 1 に示した。
陰性対照における構造異常を有する細胞の出現率は、-S9 処理および +S9 処理ともに 1.0% であった。また、倍数性異常を有する細胞の出現率は、-S9 処理および +S9 処理ともに 0.0% であった。陽性対照の MMC および B[a]P を処理した細胞では、染色分体型の切断および交換の異常が多数観察され、その出現率は 65.5% および 35.0% と陰性対照と比べて顕著な増加を示した。
GPCR を処理した細胞では、構造異常を有する細胞の出現率が、-S9 処理で 0.5~1.0%、+S9 処理で 0.0~1.5% となり、陰性対照と比較して有意な増加を示さなかった。また、倍数性異常を有する細胞の出現率は、-S9 処理および +S9 処理ともに 0.0% であり、陰性対照と比較して有意な増加を示さなかった。
連続処理法による結果を Table 2 に示した。
陰性対照における構造異常を有する細胞の出現率は、1.0% であった。また、倍数性異常を有する細胞の出現率は、0.0% であった。陽性対照の MMC を処理した細胞では、染色分体型の切断および交換の異常が多数観察され、その出現率は 47.0% と陰性対照と比べて顕著な増加を示した。
GPCR を処理した細胞では、構造異常を有する細胞の出現率が、0.0~1.0% となり、陰性対照と比較して有意な増加を示さなかった。また、倍数性異常を有する細胞の出現率は、0.0% であり、陰性対照と比較して有意な増加を
Table 1. Chromosome Aberration Test of Garcinia Powder CR: Short-term Treatment Method
| Substance | Dose ( ) | Treatment time (hr) | Recovery time (hr) | S9 mix | Number of analyzed cells | Number of structurally aberrant cells | Number of polyploid cells (%) | Cell proliferation rate (%) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| gap | ctb | cte | csb | cse | frg |
Total (%)
gap |
||||||||
| Saline | — | 6 | 18 | — | 200 | 0 | 2 | 0 | 0 | 0 | 0 | 2 (1.0) | 0 (0.0) | 100.0 |
| Garcinia Powder CR | 125 | 6 | 18 | — | 200 | 0 | 1 | 0 | 0 | 0 | 0 | 1 (0.5) | 0 (0.0) | 95.5 |
| 250 | 6 | 18 | — | 200 | 0 | 2 | 0 | 0 | 0 | 0 | 2 (1.0) | 0 (0.0) | 98.0 | |
| 500 P | 6 | 18 | — | 200 | 0 | 0 | 1 | 0 | 0 | 0 | 1 (0.5) | 0 (0.0) | 101.5 | |
| 1,000 P | 6 | 18 | — | 200 | 0 | 1 | 1 | 0 | 0 | 0 | 2 (1.0) | 0 (0.0) | 101.9 | |
| 2,000 P | 6 | 18 | — | 200 | 0 | 1 | 0 | 0 | 0 | 0 | 1 (0.5) | 0 (0.0) | 99.8 | |
| MMC | 0.1 | 6 | 18 | — | 200 | 0 | 47 | 101 | 0 | 0 | 0 | 131 (65.5)** | 0 (0.0) | 84.2 |
| Saline | — | 6 | 18 | + | 200 | 0 | 1 | 1 | 0 | 0 | 0 | 2 (1.0) | 0 (0.0) | 100.0 |
| Garcinia Powder CR | 250 | 6 | 18 | + | 200 | 0 | 1 | 0 | 0 | 0 | 0 | 1 (0.5) | 0 (0.0) | 113.1 |
| 500 | 6 | 18 | + | 200 | 0 | 2 | 1 | 0 | 0 | 0 | 3 (1.5) | 0 (0.0) | 118.4 | |
| 1,000 P | 6 | 18 | + | 200 | 0 | 0 | 0 | 0 | 0 | 0 | 0 (0.0) | 0 (0.0) | 109.1 | |
| 2,000 P | 6 | 18 | + | 200 | 0 | 0 | 0 | 0 | 0 | 0 | 0 (0.0) | 0 (0.0) | 100.4 | |
| 4,000 P | 6 | 18 | + | 200 | 0 | 1 | 1 | 0 | 0 | 0 | 1 (0.5) | 0 (0.0) | 107.9 | |
| B[a]P | 20 | 6 | 18 | + | 200 | 0 | 20 | 63 | 0 | 0 | 0 | 70 (35.0)** | 0 (0.0) | 72.5 |
ctb, chromatid break; cte, chromatid exchange; csb, chromosome break; cse, chromosome exchange; frg, fragmentation; MMC, mitomycin C; B[a]P, benzo[a]pyrene
Fisher's exact test: Significant difference from control *: , **:
P, precipitation